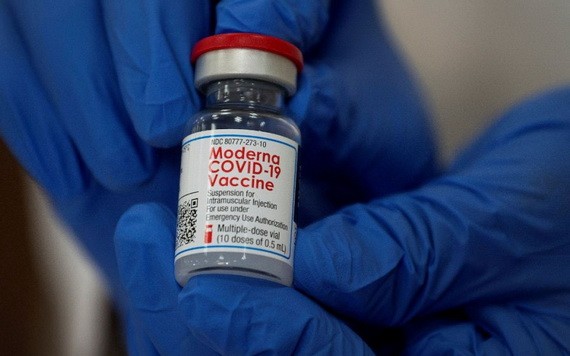
據歐盟委員會當日發佈的公告,在對疫苗安全性、有效性及質量進行全面評估後,歐洲藥品管理局對莫德納新冠疫苗給出“肯定意見”,加之歐盟各成員國也無異議,歐盟委員會決定批准莫德納新冠疫苗在歐盟市場附條件上市。公告顯示,去年11月30日莫德納公司提出上市申請之前,歐洲藥品管理局已啟動“滾動審評”對莫德納新冠疫苗進行評估,以加快審批速度;1月4日一度傳出歐洲藥品管理局或提前完成審批,但最後仍按原計劃於1月6日將審批結果公之於眾。
與德國生物新技術公司和美國輝瑞製藥有限公司研發的新冠疫苗一樣,莫德納新冠疫苗同樣使用信使核糖核酸技術(mRNA)。去年11月16日,莫德納公司宣佈其疫苗有效性達94.5%,而且無需超低溫儲存,可在2至8攝氏度的溫度中(一般冰箱冷藏室溫度)保存30天,在零下20攝氏度的溫度中保存6個月。
去年11月24日,歐盟宣佈與莫德納公司達成協議,訂購1億6000萬劑莫德納新冠疫苗,莫德納公司承諾於2021年一季度至三季度交付疫苗;按照歐盟計劃,1月6日批准使用後,如莫德納公司如期交付疫苗,歐盟隨後將在同一時間、以同等條件、按人口比例向成員國分發疫苗。
除莫德納新冠疫苗,歐盟於去年12月21日批准使用德國生物新技術公司和美國輝瑞製藥有限公司研發的疫苗,目前對該款疫苗的訂購量為3億劑;總體而言,計入與英國阿斯利康製藥公司、賽諾菲和葛蘭素史克、美國強生公司旗下楊森製藥公司、德國“痊癒”疫苗公司(CureVac)等達成的協議,歐盟現訂購近20億劑新冠疫苗,平均下來歐盟成員國每位公民約可分得4劑疫苗◆